2024.07.26
児童養護施設への寄付金活動のご報告
2024.06.27
【メディア情報】院長が執筆・監修した糖尿病の記事がYahoo!ニュースに掲載されました
2024.06.24
大人も多い!?今年流行中の「のど風邪」溶連菌感染症について
2024.06.17
「理想的なBMIは22」は本当?その理由とは
2024.05.27
2024年診療報酬改定に伴う加算に係る掲示
2024.05.09
糖尿病って遺伝する?親が糖尿病だと絶対糖尿病になるのか
2024.03.13
新型コロナウイルスワクチンの無料接種は今月まで!まだの方はお早めに
2024.03.05
【メディア情報】当院が群馬県の糖尿病内科 おすすめしたい医院として紹介されました
2024.02.06
帯状疱疹ワクチンの接種に補助金が出ます!!
2024.01.22
日本初のRSウイルスワクチン「アレックスビー」の効果や特徴は?
2024.01.04
あけましておめでとうございます
2023.12.22
X線撮影装置を更新しました(AI診断も)
2023.11.28
咳止めの飲み薬が全国的に不足しています
2023.11.14
NHKほっとぐんま630に取材協力しました
2023.11.13
えびす講市に伴う交通規制について
2023.10.24
FMぐんま「news ONE」さんから取材を受けました
2023.09.12
インフルエンザワクチンがLINEから予約可能になりました
2023.07.20
Doctors Fileより取材を受けました
2023.06.30
子どもの夏かぜ「ヘルパンギーナ」が急増中!症状と予防法は
2023.06.16
朝食抜きは体に悪いは本当か?
2023.06.06
Doctors Filmより取材を受けました
2023.05.16
インスリン代が安くなる!カートリッジ製剤について
2023.04.26
高血圧治療補助アプリCureAPP HTを導入しました―特徴や費用について解説―
2023.03.06
身体障害者補助犬の同伴受け入れについて
2023.01.16
発熱外来について(改訂版)
2023.01.05
あけましておめでとうございます
2022.10.31
えびす講に伴う交通規制について
2022.10.06
インフルエンザ予防接種について
2022.07.25
発熱外来について
2022.06.06
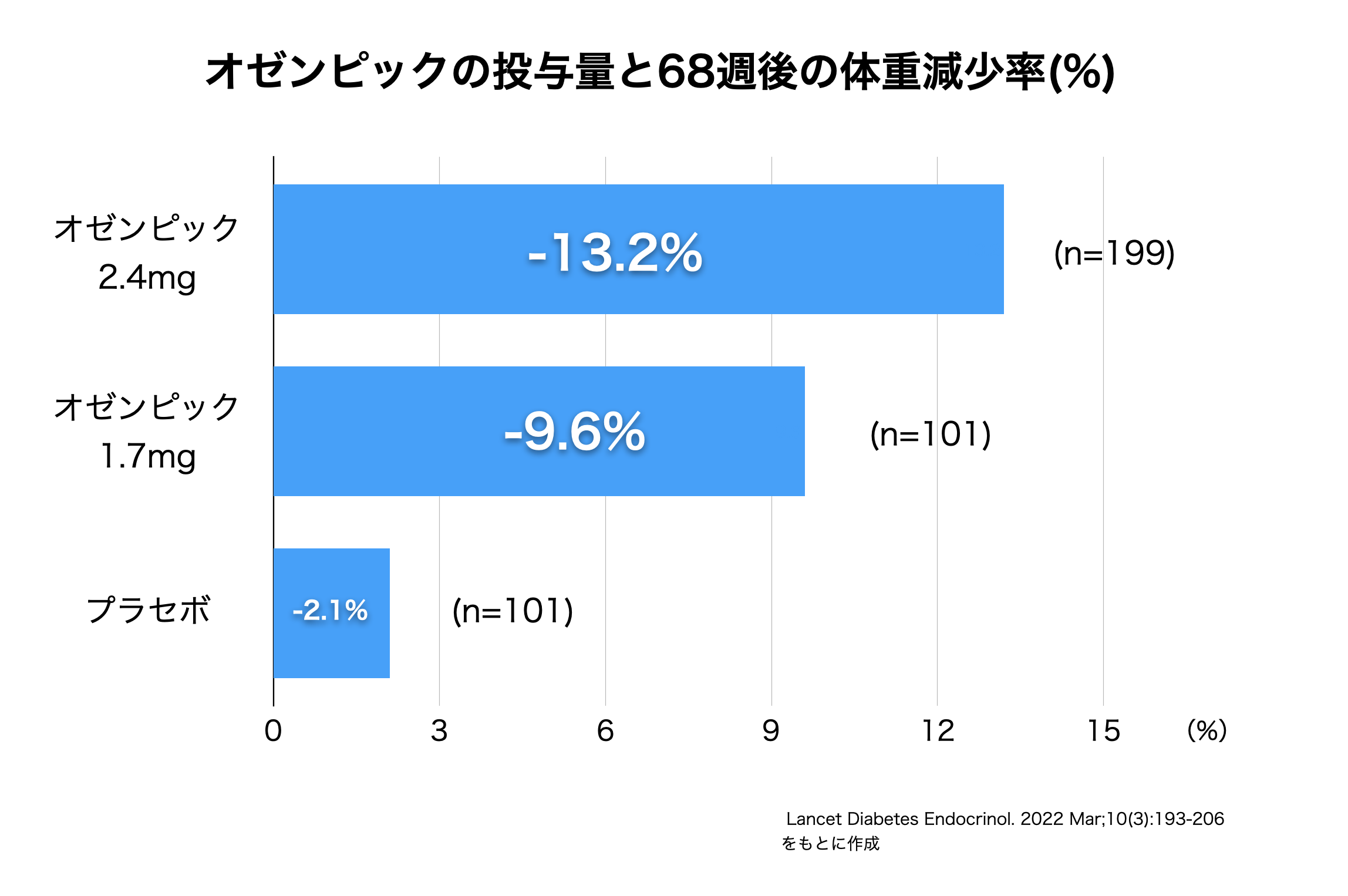
出荷調整・停止となっていたオゼンピックが新規格で発売再開!いままでとの違いは?
2022.05.20
高尿酸血症・痛風の治療ガイドラインに追補版登場。 何が追加になった?
2022.01.04
あけましておめでとうございます
2021.12.03
帯状疱疹の新型ワクチン(シングリックス)の特徴・従来ワクチンとの違いについて
2021.11.19
世界糖尿病デーとインスリン発見100周年
2021.11.11
「生涯で拍動できる心拍数は決まっている」は本当か
2021.10.06
2021年度インフルエンザワクチン接種を開始しました
2021.09.24
新型コロナワクチン接種後の懸賞?に応募してみました
2021.09.16
血圧が急に上がったけど大丈夫?一過性血圧上昇の原因と対処法
2021.09.06
【新型コロナウイルス】スパイク蛋白抗体検査について
2021.08.10
糖尿病の新薬ツイミーグ(イメグリミン)の効果と使い方
2021.07.09
ママチャリにワクチンをのせて
2021.06.18
高崎市の新型コロナウイルスワクチン接種情報についてまとめてみました
2021.05.15
【糖尿病の方へ】おすすめ記事5選
2021.04.28
思いたったが吉日:禁煙のススメ
2021.04.16
朝食を抜くと動脈硬化が悪化 理由と改善のコツ
2021.04.09
「糖尿病はやせれば治る」は本当か?
2021.04.02
睡眠時無呼吸症候群を疑う症状、なりやすい人は?
2021.03.26
心臓が大きいってどういう意味?心肥大や心拡大の原因と治療法
2021.03.19
最速の超速効型インスリン:フィアスプとルムジェブの特徴・違いについて
2021.03.12
意外と多い遺伝性の脂質異常症「家族性高コレステロール血症」の特徴・治療法
2021.03.05
血圧は1日の中で変化する。危ないパターンは?
2021.02.26
食後に血糖値があがりやすいもの・あがりにくいもの
2021.02.12
【2021年】今年の花粉は多い?少ない??
2021.01.22
心不全は繰り返す 上手な付き合い方のポイントは?
2021.01.15
2020年人気記事ベスト5
2021.01.04
あけましておめでとうございます
2020.12.25
秋冬は特に悪化注意!運動誘発喘息の特徴・予防法
2020.12.18
【糖尿病専門医が解説】低血糖の症状・原因・検査・対処法
2020.12.11
注射薬のジェネリック??バイオ後続品(バイオシミラー)について
2020.11.06
睡眠時無呼吸症候群と高血圧の「密」な関係
2020.10.23
病院で測るときだけ血圧が高い?意外と多い白衣高血圧
2020.10.16
【専門医が解説】糖尿病の運動療法
2020.10.09
【医師が解説】痛風治療薬:ユリス(ドチヌラド)の効果と副作用
2020.09.25
【専門医が解説】糖尿病の食事療法:ロカボでの糖質制限
2020.09.11
不眠症の4つのタイプ。原因と治療法は?
2020.09.04
インフルエンザの予防接種はいつから受けるべきか?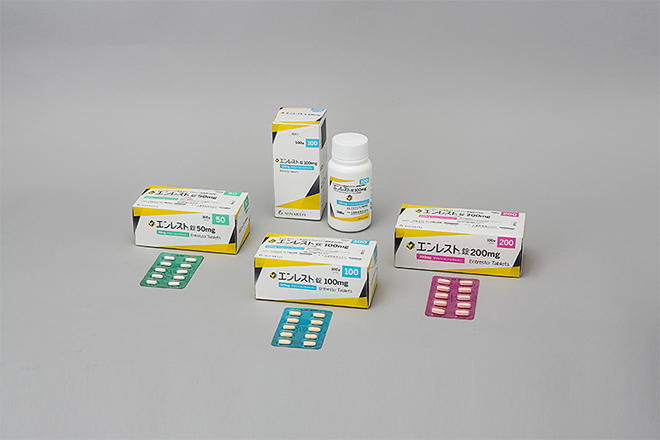
2020.08.28
心不全治療の新薬:エンレスト(サクビトリルバルサルタン)の効果と副作用
2020.08.07
内科医のできるまで(専門医取得後編)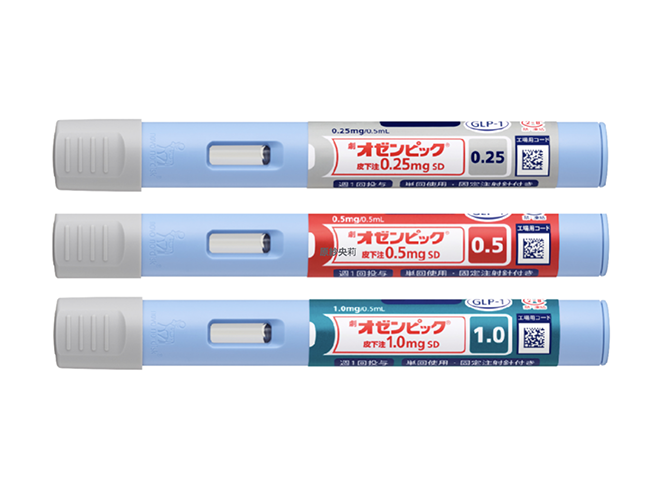
2020.07.22
【糖尿病専門医が解説】オゼンピック(セマグルチド)の効果と副作用
2020.07.17
高崎市子育て応援商品券使えます
2020.07.10
【専門医が解説】糖尿病患者さんが災害に備えてやっておくべきこと
2020.07.03
【医師が解説】便秘には3つのタイプ:原因、解消方法について
2020.06.26
【医師が解説】気管支喘息の症状、診断、治療法について
2020.06.19
【医師が解説】気圧や天候の変化と頭痛の関係:対策や治し方は?
2020.06.12
心房細動の治療薬と使い分けについて
2020.06.05
足の狭心症「閉塞性動脈硬化症」の症状・検査・治療について
2020.05.29
舌下免疫療法はいつから始めるべき?費用、効果、何歳からできる?
2020.05.22
尿検査で糖が出たら糖尿病?1+や2+の意味は?
2020.05.14
コロナ禍で外出自粛…でも予防接種や乳幼児健診の延期は危険です!
2020.04.16
いびきや睡眠時無呼吸症候群は何科を受診するべきか
2020.04.10
インスリンの正しい打ち方と管理について
2020.03.26
【医師が解説】脂質異常症治療薬:スタチン系薬の効果と副作用
2020.03.19
新型コロナウイルス感染症の影響で一部学会がオンライン併用へ
2020.03.12
内科医のできるまで(専門医編)
2020.03.04
【医師が解説】高血圧の新薬ミネブロ(エサキセレノン)の特徴と副作用
2020.02.27
糖尿病のお薬には何がある?―種類・特徴・使い分けについて
2020.02.19
内科医のできるまで(研修医編)
2020.02.06
内科医のできるまで(医大生編)
2020.01.31
入浴中の死亡は交通事故の約6倍!寒暖差やお湯の温度に注意
2020.01.28
認知症講習会で印象に残った2つの話
2020.01.27
HbA1cの測定が院内でできるようになりました
2020.01.24
【糖尿病専門医が解説】SGLT2阻害薬の効果と副作用について
2020.01.21
痛風・高尿酸血症の特徴と治療について
2020.01.17
【2020年シーズン花粉症】スギ花粉飛散量は多い?少ない?
2020.01.14
"公式版ジェネリック"オーソライズド・ジェネリック: AGを知っていますか
2020.01.09
事務スタッフの制服をリニューアルしました
2020.01.06
あけましておめでとうございます
2019.12.25
【要注意】年末年始は1年で最も糖尿病が悪化しやすい時期です
2019.12.23
糖尿病雑誌「さかえ」って知っていますか?
2019.12.16
糖尿病専門医取得しました!!
2019.11.20
「今年のインフルエンザは流行が早い」は本当!?
2019.11.11
えびす講市2019に伴う交通規制について
2019.11.06
【循環器専門医が解説】アムロジン/ノルバスク(アムロジピン)の効果と副作用
2019.10.29
インフルエンザ新薬ゾフルーザをおすすめできない理由
2019.10.03
高崎プレミアム付商品券使えます
2019.09.27
インフルエンザワクチンの中身が毎年違うって知っていました?
2019.09.11
いびきがうるさい!息が止まっている!それ病気かもしれません
2019.07.29
医学生が見学実習に来てくれました
2019.07.16
血圧脈波検査(動脈硬化の検査)で血管年齢がわかります!
2019.06.12
無料で使える街中巡回タクシー「お店ぐるりん」がはじまりました!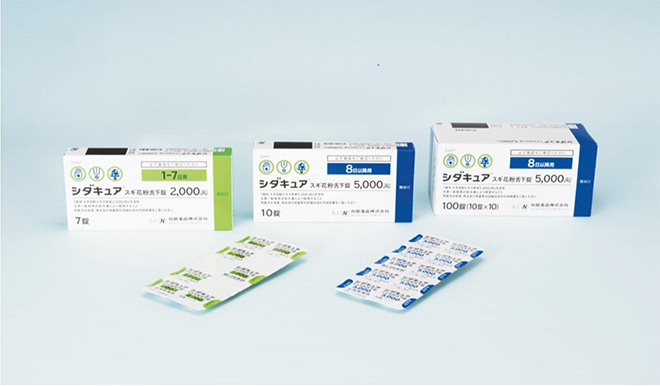
2019.06.04
舌下免疫療法の新薬「シダキュア」が5月から長期処方可能に
2019.04.02
風しんワクチン:クーポンが届いたらまずは抗体検査を
2019.03.18
こどもの花粉症:10歳未満の5人に1人は花粉症
2019.02.26
血圧の上と下の違いと脈圧について
2019.02.18
ウォーキングで老化防止!筋力低下を予防すると長生きできる!?
2019.02.04
手足が冷える!末端冷え性の原因と改善方法
2019.01.25
冬場は心筋梗塞による心停止が多発!ヒートショックを知っていますか
2019.01.19
2019年の花粉は例年と比べてやや多め!花粉症対策は飛散前から開始を
2019.01.07
あけましておめでとうございます
2018.12.20
風疹とはどんな病気?予防接種の無料期間や対象年齢は?
2018.12.07
肺炎球菌ワクチンで防げる肺炎、防げない肺炎
2018.11.20
血糖値が高いと言われたら?数値を下げる方法は?
2018.11.09
何科に行ったらわからない時はどうするべき?
2018.11.06
えびす講に伴う交通規制について
2018.10.31
降圧薬(高血圧のお薬)の種類と使い分けについて
2018.10.19
健康診断の結果などから心筋梗塞、狭心症の発症リスクがわかるアプリ、知っていますか?
2018.10.10
インフルエンザ対策:予防接種はいつから?効果・持続時間・特に必要なのは?
2018.09.28
健康診断で心電図異常を指摘されたら何科を受診するべき?どんな精密検査がある?
2018.09.18
秋なのに鼻がムズムズ。これって花粉症!?
2018.09.05
血圧の薬は一度飲み始めたらやめられないは本当か
2018.08.28
スギ花粉症が治る!?アレルゲン免疫療法(皮下・舌下免疫療法)について
2018.08.21
AED設置しました&AEDゲームの紹介
2018.08.16
かゆみ、赤み、発疹…それは食物アレルギーかもしれません
2018.08.03
明日はお祭り!交通規制にご注意下さい
2018.08.02
100人に1人はなる病気。心房細動のこと知っていますか?
2018.07.30
まずは「病名+ガイドライン」で検索!?
2018.07.27
【高血圧】どうして家庭でも血圧を測る必要があるのか
2018.07.25
糖尿病の方は年に1回は眼科受診を
2018.07.20
胸が痛い!狭心症と心筋梗塞の症状・違いとは
2018.07.16
息切れ、体のむくみ…それって心不全かも!?
2018.07.13
予防接種は親から子への大切なおくりもの
2018.07.11
【小児科】3ヶ月健診いつどこでなにをやるの?
2018.07.10
危険な不整脈とは?タイプによる危険度の違い
2018.07.09
なんとなく胸が変な感じ!?不整脈の原因と検査、治療
2018.07.06
【クリニック】プチリニューアルしました
2018.07.05
クリニックにカブトムシがやってきた!
2018.07.04
熱中症は予防が大事!しっかり対策して猛暑を乗り切ろう
2018.07.02
痛くないから大丈夫?尿酸が高いと言われたら
2018.06.26
コレステロールが高いと言われたら?数値を下げる方法は?
2018.06.19
糖尿病の方は知っておきたい。3大合併症の特徴とセルフケア
2018.06.12
高血圧について
2018.06.11
梅雨時に喘息が悪くなるのはどうして